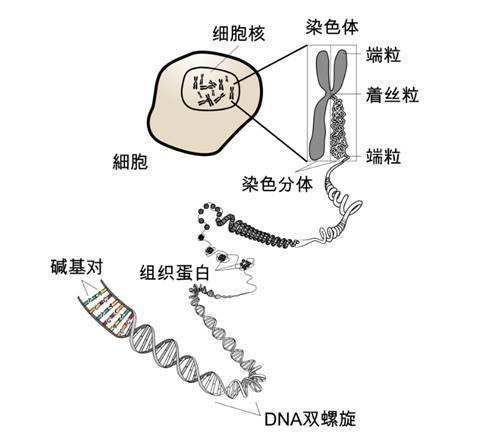
一种新的化学定义的脂质纳米颗粒可以克服腺相关病毒 (AAV) 载体在向骨骼肌提供基因组编辑疗法方面的局限性,并有望用于治疗杜氏肌营养不良症(DMD)等神经肌肉疾病。
尽管许多反义寡核苷酸疗法可用于治疗由不同突变引起的 DMD,但由于它们靶向前 mRNA 的事实,它们的效果是短暂的。
CRISPR/Cas9 基因组编辑技术前景广阔,因为它具有直接靶向 DNA 的潜力,因此具有持久的效果。
许多研究人员已使用 AAV 载体将 CRISP/Cas 9 系统引入肌肉组织。但是,这种方法存在一些问题。例如,AAV 的长表达会增加脱靶效应的风险。此外,需要多次注射才能治疗肌肉等大组织,但这对于 AAV 载体来说是不可能的,因为它们的衣壳蛋白很容易被免疫系统和中和抗体在第二次注射后攻击基因治疗注射。
目前正在研究脂质纳米颗粒作为对多种疾病具有低免疫原性的非病毒 RNA 递送载体。
在本研究中,来自日本的一组研究人员报告了一种化学定义的脂质纳米颗粒系统,能够通过重复注射将 CRISPR/Cas9 系统传递到骨骼肌。
尽管该系统的表达是短暂的,但研究人员表示,它可以在 DMD 小鼠模型中诱导稳定的基因组外显子跳跃并恢复抗肌萎缩蛋白的表达。
使用肢体灌注方法将脂质纳米颗粒引入动物体内的团队表示,该方法能够靶向多个肌肉群。
“我们的 LNP 系统的重复给药和低免疫原性是 CRISPR-Cas9 递送载体治疗骨骼肌疾病的有希望的特征,”他们写道。
CRISPR/Cas9 基因组编辑技术前景广阔,因为它具有直接靶向 DNA 的潜力,因此具有持久的效果。
许多研究人员已使用 AAV 载体将 CRISP/Cas 9 系统引入肌肉组织。但是,这种方法存在一些问题。例如,AAV 的长表达会增加脱靶效应的风险。此外,需要多次注射才能治疗肌肉等大组织,但这对于 AAV 载体来说是不可能的,因为它们的衣壳蛋白很容易被免疫系统和中和抗体在第二次注射后攻击基因治疗注射。
目前正在研究脂质纳米颗粒作为对多种疾病具有低免疫原性的非病毒 RNA 递送载体。
在本研究中,来自日本的一组研究人员报告了一种化学定义的脂质纳米颗粒系统,能够通过重复注射将 CRISPR/Cas9 系统传递到骨骼肌。
尽管该系统的表达是短暂的,但研究人员表示,它可以在 DMD 小鼠模型中诱导稳定的基因组外显子跳跃并恢复抗肌萎缩蛋白的表达。
使用肢体灌注方法将脂质纳米颗粒引入动物体内的团队表示,该方法能够靶向多个肌肉群。
“我们的 LNP 系统的重复给药和低免疫原性是 CRISPR-Cas9 递送载体治疗骨骼肌疾病的有希望的特征,”他们写道。